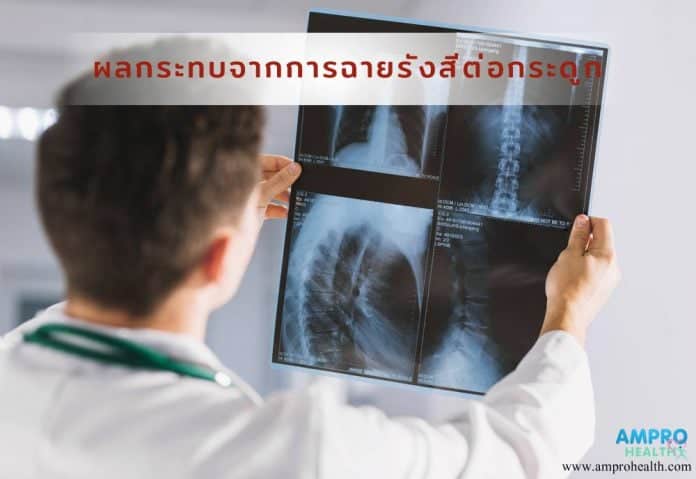
การฉายรังสีมีผลต่อกระดูก
ในปี ค.ศ.1922 Regaud เป็นผู้ที่ให้คำนิยามกับการเกิด Osteoradionecrosis ขึ้นเป็นครั้งแรก และต่อมา James Ewing ก็ได้ทำการศึกษาเกี่ยวกับการเกิดภาวะ Osteoradionecrosis พบว่าภาวะแทรกซ้อนที่เกิดขึ้นนี้เป็นสภาวะที่เกิดขึ้นได้ยากมาก แต่ว่าเมื่อเกิดขึ้นแล้วจะมีอันตรายร้ายแรงถึงชีวิตได้ ปริมาณรังสีที่จะรักษาโรคมะเร็ง สร้างความเสียหายต่อกระดูก ( Bones ) และถ้าปริมาณรังสีที่ กระดูก ได้รับมีค่ามากกว่า 5,000 จนถึง 8,000 Gy จะส่งผลให้กระดูกที่มีการเจริญเติบโตเต็มที่แล้วเกิดเน่าหรือตายลง [adinserter name=”มะเร็ง”]
จากการศึกษาของ Roher พร้อมกับคณะเกี่ยวกับ การฉายรังสี ด้วยเครื่อง Cobalt-60 เข้าสู่ร่างกายว่ามีผลกระทบใดเกิดขึ้นบ้าง พบว่าเมื่อทำการทดลองฉายรังสีเข้าสู่บริเวณขากรรไกรล่างของลิงส่งผลให้ปริมารของเยื่อ Lamella ของ กระดูก ( Bones ) ปริมาณของหลอดเลือดในเยื่อหุ้มกระดูก และจำนวนช่องของไขกระดูกมีจำนวนลดลงอย่างเห็นได้ชัด ซึ่งส่งผลให้หลอดเลือดของผู้ป่วยเกิดการอักเสบที่จะทำให้การไหลเวียนของเลือดเกิดปัญหา และถ้ามีการฉายรังสีในปริมาณที่สูงมากขึ้นอีกจะส่งผลให้เกิด Necrosis แก่ Osteoblast และ Osteocyte ที่อยู่ใน Harvesian System ที่อยู่ข้างในส่วนที่ได้รับการฉายรังสี ซึ่งจะทำให้การบวนการ Necrosis ของส่วนของกระดูก ( Bones ) และResorption ของเนื้อเยื่อ Lamella ที่เกิดการตายไปแล้วมีการทำงานที่ลดลง จึงทำให้กระดูก ( Bones ) ทำการซ่อมแซมตัวเองได้น้อยลง
ต่อมา Matsubayashi พร้อมกับคณะได้ทำการศึกษาเกี่ยวกับผลกระทบที่เกิดขึ้นจาก การฉายรังสี โดยทำการศึกษาจากศพของผู้ป่วยที่เป็นโรคมะเร็ง พบว่าเมื่อเซลล์มะเร็งตายไปและเกิด Necrosis ขึ้นแล้ว พบว่าจะมี Fibrous Tissue เข้ามาแทนที่จนสุดท้ายทั้งหมดจะถูกแทนที่ด้วย Woven bone จนกลายเป็น Lamellar bone ในลำดับสุดท้าย ซึ่งอาการแทรกซ้อนที่เกิดขึ้นนี้จะเกิดขึ้นกับผู้ป่วยหลังจากที่ได้รับการรักษาประมาณ 4 เดือน – 13 ปี การที่จะเกิดขึ้นช้าหรือเร็วก็ขึ้นอยู่กับปริมาณรังสีที่ได้รับว่ามากน้อยแค่ไหน ถ้าได้รับปริมาณรังสีมากก็จะเกิดอาการแทรกซ้อนได้เร็วกว่าผู้ป่วยที่ได้รับปริมาณรังสีน้อยนั่นเอง ภาวะ Osteoradionecrosis จะส่งผลให้กระดูกอ่อนแอลงมาก ทำให้ กระดูก ( Bones ) ไม่สามารถรับน้ำหนักตัว โดยเฉพาะในส่วนของกระดูก Long Bone ดังนั้นในขั้นตอนการทำการรักษาต้องทำการป้องกันส่วนของกระดูก เพื่อให้กระดูก ( Bones ) มีความสามรถในการซ่อมแซมตัวเองให้กลับมาสู่สภาพปกติ เช่น การทำ Internal Fixation
การเกิด Osteoradionecrosis ในผู้ป่วยจะมีลักษณะคล้ายกับการกลับมาเป็นมะเร็งซ้ำที่เกิดเนื่องจากการรักษาด้วย การฉายรังสี ซึ่งการแยกอาการทั้งสองอย่างนี้สามารถแยกได้ด้วยการตัดชิ้นเนื้อกระดูกไปทำการตรวจด้วยวิธีการ Precutaneous Needle
การเกิด Osteoradionecrosis ในส่วนของ Femoral Head จัดเป็นอาการแทรกซ้อนที่มีความรุนแรงกับผู้ป่วย ทำให้เกิด Necrosis และหลอดเลือดอักเสบเกิดขึ้นที่ส่วนต่าง ๆ ของ Femoral Head ที่มีการเกิด Necrosis ในส่วนของ กระดูก ( Bones )
[adinserter name=”มะเร็ง”] ช่วงแรกหลังจากที่ผู้ป่วยทำการฉายรังสีผู้ป่วยจะมีอาการปวดอย่างรุนแรงจนน่าตกใจ เพราะว่ากระดูกอ่อนบางส่วนได้ถูกทำลายและหลุดออกจาก Subchondral ที่อยู่ภายในข้อต่อกระดูกส่งผลให้ผู้ป่วยไม่สามารถเคลื่อน ไหวได้หรือเคลื่อนไหวได้อย่างลำบากมาก ซึ่งการเปลี่ยนแปลงที่เกิดขึ้นสามารถสังเกตได้จากการทำเอกซเรย์ MRI จะเป็นวิธีที่มีความแม่นยำค่อนข้างสูงที่จะบอกได้ว่าเป็น Avascular Necrosis ที่สามารถแสดงให้เห็นบนฟิล์มที่ทำการเอกซเรย์ สำหรับการรักษาอาการ Avascular Necrosis สามารถรักษาได้ด้วยการเจาะ Femoral Neck and Head เพื่อช่วยเร่งให้เกิด Vascular in flow ที่ช่วยกระตุ้นให้ร่างกายมีการซ่อมแซมตัวเองได้รวดเร็วขึ้นกว่าเดิม หรือจะใช้วิธีการปลูกถ่าย Free vascularized Fibular เข้าไปสู่ Femoral Neck and Head เพื่อเป็นการกระตุ้นการซ่อมแซมตัวเองให้รวดเร็วอีกวิธีหนึ่ง แต่ว่าการที่จะรักษาด้วยวิธีทั้งสองผู้ป่วยจะต้องมีกระดูกสะโพกที่อยู่ในสภาวะปกติ นอกจากทั้งสองวิธีนี้ยังมีวิธี Total Hip Replacement ที่ช่วยให้ผู้ป่วยสามารถเคลื่อนไหวได้โดยที่ไม่มีความเจ็บปวดเกิดขึ้น
นอกจากส่วนของกระดู Long Bone ที่สามารถเกิด Osteoradionecrosis ยังมี กระดูก Mandible และ Maxilla การที่จะเกิดผลกระทบนี้ก็ต่อเมื่อมี การฉายรังสี เข้าสู่บริเวณศีรษะและลำคอ อาการดังกล่าวนี้อาจจะเกิดขึ้นเองได้หรืออาจจะเกิดจากการบาดเจ็บของเนื้อเยื่อในบริเวณใกล้เคียงที่เกิดการชักนำ ทำให้เนื้อเยื่อส่วนนั้นมีความสามารถในการซ่อมแซมตัวเองได้น้อยลง และสามารถแบ่งระยะของโรคตาม
การรักษาด้วย Hyperbaric Oxygen ( HBO )
การตอบสนองต่อการรักษาด้วย Hyperbaric Oxygen ( HBO ) ได้เป็น 3 ระดับตามความรุนแรง ดังนี้
1. เห็นกระดูก Alveolar Bone ซึ่งระยะนี้จะตอบสนองต่อการรักษาดีที่สุด
2. ระยะที่ 2 เป็นระยะที่พบได้ไม่บ่อยนัก เป็นระยะที่เมื่อทำการรักษาแล้วร่างกายไม่ตอบสนองต่อการรักษา ส่งผลให้ผู้ป่วยต้องทำการผ่าตัดเอากระดูกที่เกิดการเน่าและตายออกจากร่างกาย ( Sequestrectromy/Saucerization )
3. ระยะที่ 3 เป็นระยะที่จะสังเกตเห็นแผลตลอดแนวความหนาของทุกเนื้อเยื่อ ( Full Thick Ness Involment ) หรืออาจมีอาการกระดูกกรามหักร่วมด้วย
การเกิด Osteoradionecrosis จะเกิดขึ้นก็ต่อเมื่อได้รับรังสีที่มีปริมาณ 6,000 Gy แต่โอกาสที่จะเกิดอาการข้างเคียงนี้จะยิ่งเพิ่มมากขึ้นถ้ามีการรักษาด้วยการให้ยาเคมีบำบัดร่วมด้วย ซึ่งมีข้อสันนิฐานเกี่ยวกับการเกิดได้ 2 แบบ คือ [adinserter name=”มะเร็ง”]
1. เกิดขึ้นได้เอง คือ การที่กระบวนการ Normal Turnover ของกระดูกเกิดการเปลี่ยนแปลง โดยที่มีการเกิดกระบวนการ Degradative Function เกิดขึ้นมากกว่าการเกิดกระบวนการ New Bone Production
2. เกิดเนื่องจากผลพวงจากอาการบาดเจ็บ คือ อาการข้างเคียงนี้จะเกิดจากการที่เนื้อเยื่อส่วนที่อยู่ใกล้และ กระดูก กลางในส่วนที่เคยได้รับรังสีจนไม่มีความสามารถที่จะซ่อมแซมตัวเองได้ เช่น การถอนฟัน การผ่าตัดมะเร็งหรือเนื้องอกบริเวณนี้ออกไป หรือการทำหัตกรรมที่เกี่ยวข้องกับฟันหรือทำหัตกรรมภายในช่องปาก รวมถึงการเกิดภาวะ Endarteritis ที่ทำให้เลือดและออกซิเจนไปหล่อเลี้ยงไม่เพียงพอ ทำให้เนื้อเยื่อเหงือกเน่าตายได้
Osteradionecrosis ของกระดูกกรามอธิบายได้ดังนี้ คือ เยื่อหุ้มกระดูกและเนื้อเยื่อครอบคลุมที่อยู่บริเวณด้านบนของกระดูกกรามที่มีการได้รับ การฉายรังสี ส่งผลให้เกิดภาวะ Hyperemia เกิดมี Endarteritis กับ Inflammation ซึ่งทุกสภาวะที่เกิดขึ้นนั้นจะนำไปสู่การเกิด Thrombosis จนทำให้เซลล์ตายเนื่องจากจำนวนเส้นเลือดน้อยลง ( Hypovascularity ) จนกลายเป็นพังผืด ( Fibrosis ) และเนื้อเยื่อที่เคยได้รับการฉายรังสีจะมีจำนวนเซลล์ที่ลดน้อยลงและเกิดสภาวะขาดแคลนเซลล์ชนิด Fibroblasts Osteoblasts รวมถึงขาดแคลนเซลล์ที่จะสามารถพัฒนาเป็น กระดูก ( Undifferentiated Osteocompetent Cells ) ซึ่งภาวะที่เกิดขึ้นเหล่านี้จะส่งผลต่อกระบวนการ Healing Process
อาการของภาวะกระดูกเน่าและตายที่เกิดจากการฉายรังสีในการรักษาที่เกิดขึ้นกับกระดูกกลางคือ การปวด บวม อ้าปากได้เพียงเล็กน้อย มีแผลที่เหงือกและมีการเปิดออกจนเห็นกระดูกกลางอย่างชัดเจน
อาการของ Osteoradionecrosis ที่เกิดขึ้นกับ กระดูก กลางที่เกิดขึ้น คือ การปวด บวม อ้าปากได้เพียงเล็กน้อย มีแผลที่เหงือกและมีการเปิดออกจนเห็นกระดูกกลางอย่างชัดเจน บางครั้งกระดูกกรามอาจแตกหักได้หรือมีแผลระหว่างภายในช่องปากกับส่วนของผิวหนัง ( Oral Cutaneous Fistula ) และยังพบการมี Fibrosis กับThrombosis ที่อยู่ในชั้น Intima ของส่วนของเส้นเลือดแดงที่มีหน้าที่ส่งเลือดไปหล่อเลี้ยงเยื่อที่ห่อนหุ้มกระดูกโดยเฉพาะส่งนของเส้นเลือด Inferior Alveolar Artery ที่ถือเป็นเส้นเลือดหลักที่ทำหน้าที่หล่อเลี้ยงกระดูก Mandible ในส่วนบริเวณของไขกระดูก พบว่ามีการแทนที่ด้วย Fibrous Tissue ชนิดที่มีความหนาแน่นเต็มไปหมด จนแทบจะไม่พบ Osteocytes ที่อยู่ในชั้น Cortex และยังพบว่ามีเศษเนื้อของกระดูกที่ตายไปและมีเยื่อหุ้มกระดูกที่ได้กลายเป็นพังผืดแล้วและพร้อมที่จะลอกตัวออกมาจาก Cortex เกิดขึ้นด้วย [adinserter name=”มะเร็ง”]
การรักษาภาวะ Osteoradionecrosis ที่เกิดขึ้นในส่วนของกระดูกกราม
การรักษาภาวะ Osteoradionecrosis ที่เกิดขึ้นในกระดูกกรามสามารถแบ่งออกเป็น 3 ระดับ ดังนี้
ระยะที่ 1 เป็นระยะที่แผลเปิดออกเล็กน้อย แผลค่อนข้างตื้นและสามารถมองเห็น กระดูก ที่เกิดการกร่อนไปได้ บางครั้งอาจจะมีการแยกชั้นของผิวหนังหรือในส่วนของชั้น Mucosa การทำการรักษาในระยะนี้ คือ การทำการบ้วนปากด้วยน้ำยาบ้วนปากที่ปราศจากแอลกอฮอล์ ร่วมกับการให้ยา HBO และยาปฏิชีวนะเพื่อป้องกันการติดเชื้อภายในช่อปาก ซึ่งการให้ยา HBO ในครั้งแรกจะให้ 20 Dives ก่อนเมื่อร่างกายมีการตอบสนองที่ดี นั่นคือผู้ป่วยมีอาการดีขึ้นให้เพิ่ม HBO เข้าไปอีก 10 Dives เพื่อให้เนื้อเยื่อที่เกิดการอักเสบหรือแผลที่เกิดขึ้นทำการซ่อมแซมตัวเองจนหายดี
ระยะที่ 2 ระยะนี้จะพบว่าแผลที่เกิดขึ้นมีความกว้างและลึกมากจนเห็นชั้นของ Cortical และชั้น Medullary Bone ยังพบว่ามีการฉีกขาดของMucosal และ Cutaneous ที่มีขนาดกว้างกว่าเดิม การรักษาเมื่อผลกระทบเข้ามาในระยะนี้ คือ การให้ยาปฏิชีวนะ การทำ Transoral Debridement รวมถึงการทำ Sequestr Ectomy ที่ทำการตัดเอา กระดูก ส่วนที่ตายออกไปและทำการเย็บแผลให้ติดและให้ยา HBO ร่วมด้วย จนกว่าแผลจะปิดสนิท
ระยะที่ 3 เป็นระยะที่กระดูกตลอดแนวความหนาตายไปจนถึงชั้น Inferior Border ในส่วนของกระดูกกราม ซึ่งสามารถพบว่ามี Fistula หรือกระดูกกรามแตกหัก ( Pathological Fracture ) ร่วมด้วย การรักษาเมื่อผลกระทบเข้ามาในระยะนี้ คือ ต้องทำการผ่าตัดเอาเนื้อส่วนที่ตายออกไปทั้งหมด และทำการซ่อมแซมด้วย Free Radical ในส่วนของ immediate และสามารถทำ Bone Transplant ฝั่งไว้ที่ส่วนของ กระดูก ที่ไม่เคยได้รับ การฉายรังสี มาก่อน ที่มีเลือดมาหล่อเลี้ยงเป็นปกติ ซึ่งการรักษาในระยะนี้ไม่จำเป็นต้องทำ HBO ร่วมด้วย
การเกิด Avascular Necrosis ที่ส่วนของกระดูกจากการรักษาด้วย Steroid
การรักษาด้วย Steroid ส่งผลให้เกิด Avascular Necrosis กับกระดูกได้ ผู้ป่วยประมาณร้อยละ 50-80- คนจะมีอาการแทรกซ้อนนี้เกิดขึ้นเมื่อได้รับการรักษาด้วย Steroid ซึ่งมักจะเกิดกับกระดูกสะโพกทั้งด้านขวาและด้านซ้าย จากการศึกษาในช่วงแรกพบว่าบางครั้งการเกิด Avascular Necrosis ก็ไม่มีความเกี่ยวข้องกับปริมาณของ Steroid ที่ใช้ ต่อมา Felson พร้อมกับคณะได้พบว่าปริมาณ Steroid ที่ใช้ในแต่ละวันนั้นส่งผลต่อการเกิด Avascular Necrosis อย่างชัดเจน [adinserter name=”มะเร็ง”]
การพัฒนาของโรค Avascular Necrosis เริ่มต้นด้วยการปวด ความสามารถในการเคลื่อนไหวลดลง หรือเคลื่อนได้ไม่สมดุล อาการที่เกิดขึ้นมานั้นสามารถเกิดขึ้นทั้งแบบเฉียบพลันและเกิดขึ้นในภายหลังจากที่ทำการรักษาก็ได้ และถ้าเริ่มมีอาการเกิดขึ้นแล้วอาการก็จะค่อย ๆ ลุกลามไปเรื่อยจนไม่สามารถหยุดยั้งได้ การตรวจหาว่ามีความผิดปกติเกิดขึ้นหรือไม่ต้องทำการตรวจด้วยวิธีทำ MRI จึงจะสามารถบ่งชี้ได้ในระยะเริ่มแรกที่เริ่มมีอาการเกิดขึ้น ไม่สามารถตรวจวัดได้ด้วยการเอกซเรย์แบบปกติทั่วไป โดยสังเกตจากการเปลี่ยนแปลงของ Femoral Head การตรวจวินิจฉัยเป็นสิ่งที่มีความสำคัญมาก เพราะถ้าตรวจพบได้ตั้งแต่ในระยะเริ่มต้นแล้ว จะสามารถยับยั้งการเกิดโรคไม่ให้รุนแรงมากขึ้นได้
การรักษา Avascular Necrosis ที่ดีที่สุดเมื่อทำการพบในระยะเริ่มแรก คือ การทำ Core Decompression เพื่อที่จะลดแรงกดที่อยู่ภายใน Medullary เพื่อหยุดหรือย้อนกลับกระบวนการที่ทำให้เกิดโรค Avascular Necrosis ต่อมา Wang กับคณะได้ทดลองทำการ Decompression ในกระต่าย พบว่าช่วยทำให้การไหลเวียนของเลือดที่ส่วนของ Femoral Head กลับเข้าสู่สภาวะปกติ ซึ่งสามารถทำให้เกิดปฏิกิริยาย้อนกลับของ Avascular Necrosis หรือที่เรียกว่า Revascularization
แต่ทว่าในปัจจุบันนี้การตรวจพบ Avascular Necrosis จะตรวจพบในระยะที่มีการพัฒนามาเป็น Avascular Necrosis เต็มตัวแล้ว การรักษาให้หายจึงเป็นไปได้ยาก ทำให้แต่ Total Hipreplacement เพื่อช่วยบรรเทาอาการเจ็บปวดที่เกิดขึ้นและช่วยให้ผู้ป่วยสามารถเคลื่อนไหวตัวได้มากขึ้นเท่านั้นเอง
การเกิดมะเร็งทุติยภูมิชนิด Sarcoma ที่มีสาเหตุมาจากการฉายรังสี
การรักษาโรคมะเร็งมีความสำเร็จเกิดขึ้นมากมาย ส่งผลให้มีผู้ป่วยที่รอดชีวิตจากโรคมะเร็งเป็นจำนวนมากและมีอายุยืนยาวมานับสิบสิบปี แต่บางครั้งผู้ป่วยที่รอดชีวิตจากการรักษาโรคมะเร็งด้วย การฉายรังสี พบว่ามีการเกิดเป็น Sarcoma เพิ่มมากขึ้น Sarcoma จะเกิดขึ้นเมื่อผู้ป่วยมีอายุประมาณ 60 ปี เมื่อเกิด Sarcoma แล้วจะมีอาการบวมร่วมด้วย ซึ่งการเกิดอาการดังกล่าวจะเกิดขึ้นอย่างเฉียบพลันในส่วนของกระดูกที่เคยเจ็บป่วยมาก่อน
ซึ่งการที่ผู้ป่วยจะมีการพัฒนากลายเป็น Sarcoma ได้นั้นต้องอาศัยระยะเวลาอย่างน้อย 20 ปีขึ้นไป และการฉายรังสีที่จะส่งผลให้ผู้ป่วยเกิด Sarcoma ได้นั้นต้องมีความเข้มข้นของรังสีมากกว่า 300 Gy และมีการฉายรังสีนานเกิน 28 วัน แต่ถ้าได้รับปริมาณรังสีน้อย ๆ ก็ต้องได้รับรังสีเป็นระยะเวลาที่นานมากจึงจะส่งผลกระทบให้เกิด Sarcoma ได้ การเกิด Sarcoma นี้สามารถเกิดขึ้นได้กับ กระดูก ( Bones ) ทุกส่วนของร่างกายรวมถึงเนื้อเยื่ออ่อนก็มีโอกาสที่จะเกิดได้เช่นกัน
เราไม่สามารถแยกความแตกต่างระหว่าง Sarcoma ที่เกิดขึ้นหลังจากที่ได้รับการรักษาด้วย การฉายรังสี กับ Osteogenic Sarcoma ชนิดที่เรียกว่า Idiopathic ที่อาจจะเกิดขึ้นได้เอง ซึ่งการสันนิฐานว่าเป็นมะเร็งชนิดใด ต้องอาศัยการดูประวัติย้อนหลังของผู้ป่วยที่เข้ารับการรักษาร่วมด้วย จากการเอกซเรย์เราสามารถเห็นลักษณะเฉพาะบางแบบที่เกิดขึ้นในส่วนของกระดูก ( Bones ) ที่ถูกทำลายไปและมีการซ่อมแซมขึ้นมาใหม่ ซึ่งที่กระดูส่วนนี้จะมีความหนาแน่นที่ไม่สูงมาก โดยจะค่อย ๆ เกิด Periosteal Elevation ในขณะที่ก้อนเนื้อจะเกิดในส่วนของ Soft Tissue จึงเป็นเรื่องยากที่เรายะทำการแยกความแตกต่างระหว่างการเปลี่ยนแปลงของ nercrosis ที่เกิดขึ้นหลังจากที่ได้รับการฉายรังสี แต่ในการเกิด Osteogenic Sarcoma ชนิดที่เรียกว่า Idiopathic จะไม่มีลักษณะดังกล่าวเกิดขึ้น ดังนั้นการตรวจว่าเป็นมะเร็งชนิดใดสามารถทำได้ด้วยการตัดเอาชิ้นเนื้อไปตรวจเพียงวิธีเดียวเท่านั้นที่จะสามารถแยกมะเร็งทั้งสองชนิดออกจากกันได้สำหรับผู้ป่วยที่เกิดเป็น Sarcoma ภายหลังจากที่ได้รับการรักษานั้นจะมีโอกาสรอดชีวิตที่น้อยมาก และเมื่อเกิด Sarcoma จะมีชีวิตอยู่ได้เพียง 1 ปีหลังจากที่อาการแสดงออกมา ซึ่งผู้ป่วยมีอัตราการรอดชีวิตจากโรคนี้แค่ร้อยละ 1-2 เท่านั้น [adinserter name=”มะเร็ง”]
ผู้ป่วยที่เป็น radiation Induced Osteogenic Sarcoma นิยมรักษาด้วยการผ่าตัดและการให้เคมีบำบัดในการรักษา แต่ไม่นิยมใช้ การฉายรังสี ร่วมด้วยในการรักษา ถึงแม้ว่าการเกิด Sarcoma จะมีอัตราการเกิดที่น้อยมาก แต่ว่าถ้ามีอาการแทรกซ้อนเกิดขึ้นแล้ว จะเป็นอันตรายต่อตัวผู้ป่วยเป็นอย่างมาก จึงไม่ทำการรักษาด้วยการฉายรังสี นอกจากเป็นกรณีที่มีความจำเป็นต้องจริง ๆ เท่านั้น
การแพร่กระจายของมะเร็งเข้าสู่มดลูก
ปัจจุบันนี้ผู้ป่วยที่รอดชีวิตจากการเป็นมะเร็งมีจำนวนเพิ่มขึ้นจากในอดีต แต่ว่าผู้ป่วยที่รอดชีวิตจากการรักษาโรคมะเร็งนั้นมีความถี่ในการเกิดแตกหักของ กระดูก ที่เป็นโรคอื่น ๆ ( Pathological Fracture ) อยู่แล้วเกิดขึ้นเป็นจำนวนมาก พบว่ามะเร็งที่เต้านมเป็นมะเร็งที่มีการแพร่กระจายเข้าไปสู่กระดูกมากที่สุด มากถึงครึ่งหนึ่งของผู้ป่วยที่มีการกระจายตัวของมะเร็งเข้าสู่กระดูกเลยทีเดียว การกระจายตัวจะกระจายแบบ Lytic Lesions และสามารถพัฒนาไปเป็น Sclerotic Lesions ที่สามารถพบได้บ่อยในมะเร็งต่อมลูกหมาก มะเร็งกระเพาะปัสสาวะ มะเร็งที่เกี่ยวข้องกับระบบทางเดินอาหาร ทั้งนี้ยังมีการเกิดรอยโรคที่ส่วนของกระดูกได้อีกด้วย ทั้งแบบ Sclerotic และ Lytic ซึ่งพบมากในกรณีที่เป็นมะเร็งเต้านม
การแพร่กระจายของมะเร็งสามารถแพร่กระจายเข้าสู่กระดูกได้ทุกส่วน โดยมักจะเริ่มจากการกระดูกที่มีต้นกำเนิดอยู่ที่ไขกระดูกแดงเป็นอันดับแรกก่อน จึงจะแพร่เข้าไปใน Infilrate ที่อยู่ใน Cortex ของกระดูก ซึ่งจะส่งผลกระทบต่อ Axial Skeleton มากกว่าที่จะส่งผลกระทบต่อ Appendicular Skeleton ทางการแพทย์จะใช้ Bone Scintigraphy ในการบอกตำแหน่งที่มีการแพร่กระจายของมะเร็งที่เกิดขึ้นแต่ละชนิดได้ และยังเป็นการตรวจสอบที่มีประโยชน์มาก และยังสามารถตรวจ Bone Secondaries ที่มีขนาดเพียง 10 ml ได้ นอกจากนั้นยังสามารถใช้วิธี Emission Isoto Pic Tomographic Scintigraphy ในการตรวจรอยโรคแพ้ที่มีขนาดเล็กมากถึงขนาด 2 ml ได้อีกด้วย
ผู้ป่วยที่ป่วยเป็นมะเร็งเต้านมที่อยู่ในระยะลุกลามจะมีอการเจ็บปวดเกิดขึ้นเป็นส่วนมาก แต่ก็มีส่วนน้อยที่อาการปวด บวมจะไม่แสดงอาการออกมา และอาการแรกที่บ่งบอกว่ามะเร็งมีการแพ่กระจายไปสู่ส่วนของ กระดูก แล้วเป็นอาการ Pathological Fracture ซึ่งสามารถทำการตรวจสอบได้ด้วยเทคนิค Scintigraphy ที่มีการใช้ Technetium-99m เข้ามาในการตรวจสอบ ที่เป็นเช่นนั้นก็เพราะว่าการแพร่กระจายของมะเร็งนั้นมีลักษณะเป็น Multifocal นั่นเอง
ผู้ป่วยที่เป็นมะเร็งเต้านมที่อยู่ในระยะที่มีการแพร่กระจายแล้ว เมื่อทำการตรวจสอบเปรียบเทียบระหว่าง X-ray Bone Scan กับการทำ CT Scan พบว่าการทำ CT Scan นั้นสามารถทำการแยกความแตกต่างระหว่างโรคข้อเสื่อมกับลักษณะของมะเร็งที่เกิดการแพร่กระจายได้ แต่ถ้าการทำตรวจสอบด้วยเทคนิค Technetium-99m จะไม่เห็นความแตกต่างระหว่างว่าเป็นการแพร่กระจายของมะเร็งหรือเป็นโรคข้อเสื่อม ทางด้านการตรวจทาง Metabolic นั้นไม่มีประโยชน์ต่อการประเมินเพื่อบ่งบอกว่าอาการที่เกิดขึ้นเป็นอะไร [adinserter name=”มะเร็ง”]
ความเจ็บปวดที่เกิดขึ้นนั้นส่งผลต่อการดำรงชีวิตประจำวันของผู้ป่วยเป็นอย่างมาก โดยเฉพาะอย่างยิ่งถ้ากระดูกต้องทำการรับน้ำหนักมาก ๆ ซึ่งอาการปวดสามารถบรรเทาได้ด้วย การฉายรังสี แต่ถ้าทำการฉายรังสีนานเข้าจากที่ทำการฉายแล้วจะหายปวดในทันทีก็จะกลายเป็นว่าความเจ็บปวดจะอยู่นานขึ้นกว่าครั้งแรกที่ทำการฉายรังสี นั่นแสดงว่ามะเร็งที่เป็นอยู่เกิดการดื้อต่อการฉายรังสี
กระดูก จะมีการตอบสนองหลายแบบมากเพื่อที่กระดูกจะได้เข้าสู่กระบวนการ Reossifcation ถ้าหลังจากที่รักษาด้วยการฉายรังสีแล้วเกิดมีรอยโรคแบบ Lytic เกิดขึ้นมา อัตราในการเกิดกระบวนการ Reossifcation หลังจากที่ทำการรักษาแล้วจะอยู่ที่ประมาณ 35-80 % ซึ่งสามารถลำดับเหตุการณ์ที่เกิดขึ้นได้ดังนี้ เริ่มจากการเกิด Necrosis ภายในเซลล์มะเร็ง และเริ่มมีการ Proliferation ของส่วน Fibrous Tissue เข้าไปใน Woven Bone ซึ่งจะสามารถพัฒนาต่อไปเป็น Lamellar Bone ในเวลาต่อมาได้ ซึ่งถ้าอยู่ในสภาวะปกติ Woven Bone จะไม่สามารถพัฒนาไปเป็น Lamellar Bone ได้เลย
สำหรับผู้ป่วยบางส่วนจะมีอาการแทรกซ้อนเกิดขึ้นได้ ดังนั้นจึงต้องทำ Prophylactic Internal Fixation เพื่อไม่ให้เกิดอาการแทรกซ้อนขึ้นมา ซึ่งการทำ Prophylactic Internal Fixation จะขึ้นอยู่กับความเสี่ยงต่อการเกิด Pathological Fracture โดยที่อัตราการเกิด Pathological Fracture จะมากหรือน้อยก็ขึ้นอยู่กับระดับของ Cortical Destruction โดยเฉพาะส่วนในของกระดูก Long Bone นั่นคือถ้า Cortical Destruction มีระดับมากกว่า 50 % แล้วจะส่งผลให้มีความถี่ในการเกิด Pathological Fracture ทำให้มี Pathological Fracture เพิ่มขึ้นอย่างเฉียบพลัน นอกจากนี้ยังมีตัวบ่งชี้อีกอย่างที่ต้องทำการ Fixation นั่นคือการปวดที่กระดูกอย่างต่อเนื่อง แม้ว่า Long Bone จะยังคงหลงเหลืออยู่และถึงจะทำ การฉายรังสี แล้วก็ตาม
การเกิด Pathological Fracture มักจะเกิดการสะสมจาก Microfracture หลายจุด ซึ่งบางครั้งก็ไม่สามารถที่จะหลีกเลี่ยงได้ ซึ่งมีความสัมพันธ์กับค่าน้ำหนักที่ต้องกดลงบนส่วนดังกล่าวในขณะที่ทำการเคลื่อนไหวหรือเดิน ดังนั้นเมื่อเกิดรอยแตกที่มีขนาดเส้นผ่าศูนย์กลาง 2.5 ml ในบริเวณProximal Femur หรือแม้กระทั่งการมี Pathological Avulsion ในส่วนของ Lesser Trochanter ทั้งหมดนี้ต่างเป็นตัวบ่งชี้ว่า Femur นั้นมีความอ่อนแอลงเป็นอย่างมาก และมีแน้วโน้มที่ว่าจะสามารถพัฒนาไปเป็น Pathological Fracture ในอนาคตได้ ดังนั้นจึงจำเป็นต้องทำ Internal Fixation เพื่อที่จะเข้าไปช่วยในการพยุงกระดูกและป้กงักนไม่ให้กระดูกเกิดการบาดเจ็บในอนาคตได้ และยังต้องทำการฉายรังสีเข้าสู่กระดูกต่อไปเพื่อป้องกันไม่ให้กระดูกถูกทำลายเพิ่มขึ้นอีก [adinserter name=”มะเร็ง”]
จึงสรุปได้ว่าการทำ Pathological Fixation เป็นสิ่งที่ดีสำหรับตัวผู้ป่วย เพราะสามารถช่วยลดความเสี่ยงในการเกิด Fixation และช่วยประคองอาการของผู้ป่วยไม่ให้แย่ลงไปกว่าเดิม ทำให้ผู้ป่วยรู้สึกเจ็บปวดน้อยลง เคลื่อนไหวได้มากขึ้น ส่งผลให้ผู้ป่วยสามารถใช้ชีวิตประจำวันได้อย่างปกติสุข
Pathological Fracture
พบว่าการเกิด Pathological Fracture ในบริเวณของกระดูกสันหลังและ กระดูก Long Bone จะส่งผลให้ผู้ป่วยได้รับความเจ็บปวดอย่างรุนแรงและร่างกายบางส่วนต้องสูญเสียประสิทธิภาพในการทำงานไป ซึ่งอาจเกิดขึ้นได้ทั้งในขณะที่ทำการรักษาหรือหลังจากที่ได้รับการรักษาแล้ว ที่เป้ฯเช่นนั้นก็เพราะว่ารังสีทำให้เกิดกสภาวะกระดูกมีรูพรุน ที่มีส้าเหตุมาจากการเกิด Hyperaemie ที่มีปริมาณเพื่อขึ้นชนิดชั่วคราวทำให้กระดูกมีความแข็งแรงลดลง ส่งผลให้กระดูกที่มีการแพร่กระจายของมะเร็งเข้าเกิดการแตกหัก ซึ่งในปัจจุบันนี้ยังไม่สามารถระบุความสัมพันธ์ที่แน่ชัดของการเกิด Pathological Fracture กับปริมาณรังสีว่ามีความสัมพันธ์กันอย่างไร แต่ก็พบว่ามีการเกิด Pathological Fracture หลังจากที่ได้รับ การฉายรังสี เกิดขึ้นได้
ซึ่งเป้าหมายของการรักษา Pathological Fracture ก็คือ ความต้องการที่จะรักษาสภาพของ Fragment ให้อยู่ในสภาวะปกติให้ได้มากที่สุด เพื่อที่กระดูกจะได้มีความแข็งแรงที่เพียงพอในการเคลื่อนไหวของร่างกายให้ได้โดยที่ไม่เจ็บปวดและไม่ใช้เครื่องช่วยพยุงด้วย เพื่อที่ผู้ป่วยจะสามารถดำรงชีวิตได้เหมือนคนทั่วไป
การ Fixation กับกระดูก Long Bone ที่มีการเกิด Fracture ต้องได้รับการดูแลสภาพของ กระดูก ตลอดทั้งชิ้นไม่ใช่ทำการดูแลเฉพาะส่วนใดส่วนหนึ่งเท่านั้น โดยที่ fractures เข้าไปที่ Proximal Femur ด้วยวิธี Joint Replacement ในขณะที่ส่วนของ Shaft fractures นั้นควรได้รับการรักษาด้วยวิธีการ Intramedullary Nailinl ที่มีการใช้ Interlocking Nail ในส่วนหรือในจุดที่ทำการระบุเอาไว้ ซึ่งจะช่วยพยุงกระดูกทั้งชิ้นและ Nail ยังสามารถใส่ด้วยเทคนิคปิดที่จะทำให้ผู้ป่วยได้รับความเจ็บปวดน้อยลงด้วย
บางครั้งการ Fractures Lytic ที่มีขนาดใหญ่มากเมื่อทำการ Fixation ก็อาจจะทิ้งร่องรอย Defect ที่มีขนาดใหญ่ตามไปด้วยแต่ก็มีเพียงแค่วิธี Fixation Device เท่านั้นที่จะสามารถช่วยพยุงร่างกายเอาไว้ได้ ซึ่งเมื่อผ่านไปเป็นเวลานานขึ้น การทำ Fixation Device จะส่งผลให้เกิดอาการอ่อนล้า ส่งผลให้มี Fractures เพิ่มมากขึ้นเรื่อยจนในที่สุด กระดูก ก็จะเกิดการแตกหักได้ในที่สุด เพื่อป้องกันอาการดังกล่าวที่จะเกิดขึ้นจึงมีการทำ Methyl Methacrylate Cement ที่สามารอุดรอย Defect ที่อาจเกิดขึ้นมาได้ เป็นการช่วยพยุงส่วนรอบ ๆ Fixation Device ซึ่งทำการเชื่อมต่อด้วย Cement เมื่อ Cement แข็งตัวแล้ว ผู้ป่วยก็จะทำการเคลื่อนไหวร่างกายได้ และการเติม Cement เข้าไปในส่วนของรอย Defect นั้นยังช่วยป้องกันแรงกดทับที่จะเข้ามาสร้างความเสียหายให้กับ Fragment ที่ส่วนต่าง ๆ และช่วยผ่อนการทำงานของ Fixation Device ซึ่งการใช้ Cement ในผู้ป่วยไม่ควรใช้ในผู้ป่วยที่คาดว่าจะมีอายุรอดต่ำกว่า 3 เดือน[adinserter name=”มะเร็ง”]
พบว่าการรักษา Pathological Fracture ที่ทำอยู่ในปัจจุบันนี้เป็นวิธีที่ดีที่สุด ที่ช่วยลดความเจ็บปวดที่เกิดขึ้นและยังสามารถช่วยให้ผู้ป่วยเคลื่อนไหวร่างกายได้มากขึ้น ซึ่งสำหรับผู้ป่วยแล้วแนวทางการรักษาที่ใช้อยู่ในปัจจุบันนี้เป็นแนวทางที่ดีสุดแล้ว ถึงแม้ว่าเมื่อผู้ป่วยเกิดอาการ Pathological Fracture หลังจากที่ได้รับการรักษาด้วย การฉายรังสี แล้วจะมีโอกาสรอดชีวิตน้อยมากก็ตาม แต่การรักษา Pathological Fracture ที่ใช้อยู่ก็สามารถยืดชีวิตผู้ป่วยออกไปได้อีกระยะเวลาหนึ่งอีกด้วย
ดังนั้นวิธีการที่ดีที่สุดก็คือการป้องกันไม่ให้อาการข้างเคียงอย่าง Pathological Fracture เกิดขึ้นกับผู้ป่วยที่ทำการรักษาด้วย การฉายรังสี ทั้งที่เกิดขึ้นในขณะที่ทำการฉายรังสีและหลังจากที่ได้รับการฉายรังสีไปแล้ว จึงจะเป็นหนทางที่ดีที่สุดสำหรับตัวผู้ป่วยและทีมแพทย์ที่ทำการรักษา
ร่วมตอบคำถามกับเรา
อ่านบทความที่เกี่ยวข้องเพิ่มเติมตามลิ้งค์ด้านล่าง
เอกสารอ้างอิง
ศาสตราจารย์เกียรติคุณ แพทย์หญิงพวงทอง ไกรพิบูลย์. รู้ก่อนเข้าใจการตรวจรักษามะเร็ง. กรุงเทพฯ: ซีเอ็ดยูเคชั่น, 2557.
Bahadur, G. (2000). “Age definitions, childhood and adolescent cancers in relation to reproductive issues”. Human Reproduction. 15: 227. doi:10.1093/humrep/15.1.227.