เสริมจมูก
การผ่าตัด เสริมจมูก เพื่อนำวัสดุหรือสิ่งแปลกปลอมจากภายนอกร่างกาย (Foreign Body materials) เข้าสู่ร่างกายย่อมมีความเสี่ยงที่ร่างกายจะเกิดปฏิกิริยาการต่อต้านจากร่างกายอย่างแน่นอน แต่ปฏิกิริยาดังกล่าวจะเกิดขึ้นมากหรือน้อยก็ขึ้นอยู่กับความแข็งแรงและวัสดุที่นำเข้ามาใช้ในการเสริมจมูกด้วย ซึ่งวัสดุที่นำมาเสริมจมูกมีทั้งเนื้อเยื่อที่มาจาก
ธรรมชาติและวัสดุที่มาจากการสังเคราะห์ทางวิทยาศาสตร์ การนำเนื้อเยื่อสามารถนำมาได้จากผู้บริจาคอื่นและการนำเนื้อเยื่อมาจากอวัยวะอื่นภายในร่างกาย ซึ่งเนื้อเยื่อที่นำมาจากอวัยวะส่วนอื่นนั้นถึงแม้ว่าร่างกายจะไม่มีปฏิกิริยาต่อต้านเกิดขึ้นแต่ว่าผู้เข้ารับการผ่าตัดก็ต้องเจ็บตัวเนื่องจากการนำเนื้อเยื่อดังกล่าวมาใช้ จึงกล่าวได้ว่าต้องเจ็บตัวถึงสองครั้งในการ เสริมจมูก เพียงที่เดียว และบางครั้งปริมาณของเนื้อเยื่อหรือกระดูกที่มีอยู่ไม่เพียงพอต่อความต้องการใช้ในการเสริมจมูก จำเป็นต้องใช้วัสดุสังเคราะห์ร่วมด้วย ส่วนวิธีการเสริมจมูกด้วยการเติมวัสดุเข้าไปที่บริเวณด้านบนหรือด้านล่างของจมูก สามารถแบ่งออกเป็น 2 กลุ่มตามลักษณะขั้นตอนการทำ คือ
1.การผ่าตัดเสริมจมูกด้วยวัสดุแบบแท่ง
2.การเสริมจมูกด้วยการฉีดสารเติมเต็ม ( Filler )
การเสริมจมูกด้วยการฉีดสารเติมเต็ม ( Filler )
การทำจมูกหรือ เสริมจมูก ด้วยการฉีดสารเติมเต็ม ( Filler ) คือ การฉีดเพื่อนำวัสดุเข้าสู่อวัยวะของร่างกาย วัสดุจะต้องอยู่ในรูปของเหลว เช่น น้ำ วุ้นหรือผงขนาดเล็กที่สามารถนำมาผสมน้ำหรือตัวทำละลายอื่นให้กลายเป็นของเหลว เพื่อที่จะสามารถทำการฉีดผ่านเข็มเข้าไปสู่จมูกได้ ซึ่งสารที่สามารถนำมาฉีดเข้าไปในร่างกายแบ่งออกเป็น 2 กลุ่ม ดังนี้
[adinserter name=”ศัลกรรมความงาม”]
1.ของเหลวที่สามารถฉีดเข้าไปแล้วสามารถคงอยู่ได้ตลอดไป ( Permanent Filler )
สารชนิดนี้มีคุณสมบัติที่สามารถคงตัวอยู่หรือกระจายตัวอยู่ในเนื้อเยื่อของคนไข้ได้ตลอดไป ซึ่งในระยะแรกกลังจากที่สารนี้เข้าไปแล้วลักษณะโดยรวมของจมูกจะดูสวยงาม แต่เมื่อผ่านไปสักระยะหนึ่งแล้ว ร่างกายจะรู้ว่าได้รับสิ่งแปลกปลอมเข้ามาย่อมเกิดปฏิกิริยาการต่อต้านขึ้น เช่น การอักเสบ บวมแดง ซึ่งอาการดังกล่าวจะเป็น ๆ หาย ๆ บางครั้งร่างกายจะทำการสร้างพังผืดที่มีลักษณะคล้ายเส้นใยมาห่อหุ้ม ส่งผลให้มีลักษณะเป็นก้อนที่มีผิวเป็นตะปุ่มตะป่ำ การรักษาอาการที่เกิดขึ้นเป็นไปได้ยาก ซึ่งสารที่ทำให้เกิดอาการดังกล่าว คือ ซิลิโคนเหลว พาราฟินและซิลิโคนหงส์ที่ต้องนำมาผสมน้ำ ( Bioplastic )
2.ของเหลวที่สามารถฉีดเข้าไปแล้วสามารถละลายหายไปได้เอง
สารจำพวกนี้ได้มีการคิดค้นเพื่อให้สามารถคงอยู่ภายในร่างกายได้ประมาณ 1 ปี แล้วจึงจะสลายตัวไป เนื่องจากถ้าให้คงอยู่ยาวนานกว่านี้จะก่อให้เกิดอันตรายต่อร่างกาย ซึ่งไม่สามารถทำการรักษาให้หายได้ ซึ่งการฉีดสารเติมเต็มเข้าสู่
จมูกเพื่อทำการ เสริมจมูก ต้องทำโดยแพทย์ที่มีความชำนาญในการฉีดที่สูงมาก เนื่องจากหากเกิดความผิดพลาดในการฉีด เช่น การฉีดเข้าไปในเส้นเลือด ตา โพรงจมูกแล้ว อาจส่งผลให้เส้นเลือดอุดตัน เนื้อเยื่อที่อวัยวะเกิดการเน่าหรือตายได้ ถ้าหากเข้าไปในดวงตาอาจทำให้ดวงตามองไม่เห็นหรือตาบอดได้ และระหว่างที่สารนี้ยังสลายไปไม่หมด อาจก่อให้เกิดอาการแทรกซ้อนหรือโรคแทรกซ้อนกับร่างกายได้ เช่น การอักเสบ การบวมแดง ผิวหนังมีลักษณะที่ขรุขระ สารเติมเต็มที่อยู่ในกลุ่มนี้ เช่น Hyalutonic acid เป็นต้น
การเสริมจมูกด้วยการฉีดสารเติมเต็ม เป็นการฉีดเพื่อนำวัสดุเข้าสู่อวัยวะของร่างกาย วัสดุจะต้องอยู่ในรูปของเหลวเพื่อให้สามารถผ่านเข็มเข้าสู่จมูก
อาการแทรกซ้อนที่เกิดขึ้นจากการเสริมจมูกที่พบได้บ่อย
การ เสริมจมูก สามารถสร้างจมูกที่มีรูปทรงที่สวยงาม ส่งผลให้ใบหน้ามีมิติน่ามองยิ่งขึ้น แต่ว่าการผ่าตัดเพื่อเสริมจมูกใช่ว่าจะมีแต่ข้อดีเพราะว่าในการผ่าตัดย่อมมีความเสี่ยงที่จะเกิดอาการแทรกซ้อนเกิดขึ้น ซึ่งอาการแทรกซ้อนที่เกิดขึ้นจากการทำจมูกที่พบได้บ่อยครั้ง คือ
1.การติดเชื้อ
การผ่าตัดที่ไม่สะอาดหรือการผ่าตัดที่ไม่ได้ตามมาตรฐาน ทั้งจากความชำนาญของแพทย์ ความสะอาดของสถานที่ผ่าตัด ความสะอาดและวัสดุที่นำมา เสริมจมูก ล้วนเป็นปัจจัยที่ส่งผลให้เกิดความเสี่ยงในการติดเชื้อได้ทั้งสิ้น การติดเชื้อสามารถแบ่งออกได้เป็น 3 ระยะ ดังนี้
ระยะแรก คือ ระยะหลังจากที่ทำการผ่าตัดเสร็จสิ้น ผู้ป่วยจะมีอาการปวดแสบปวดร้อน บวมแดง เนื่องจากการผ่าตัดที่มีความสะอาดน้อย หรือมีเลือดคั่งบริเวณจมูกหรือภายในโพรงจมูกซึ่งมีเชื้อโรคอยู่ภายในนั้น เช่น ผู้ป่วยที่มีอาการไซนัสอักเสบ ซึ่งหากมีอาการดังกล่าวเกิดขึ้นแล้ว แพทย์จะต้องรีบนำสิ่งแปลกปลอมที่มีอยู่ในจมูกออกมาและทำความสะอาดแผลทันที พร้อมทั้งให้ยาปฏิชีวนะเพื่อรักษาอาการอักเสบที่เกิดขึ้น
การติดเชื้อระยะที่สั้น คือ ระยะหลังจากผ่าตัดประมาณสัปดาห์ที่ 2 ถึงสัปดาห์ที่ 4 ลักษณะอาการจะคล้ายคลึงกับอาการในระยะแรก คือ มีอาการเจ็บ แดงและบวมเกิดขึ้นก่อนที่จะมีน้ำเหลืองไหลหรือน้ำหนองไหลออกมาจากแผลที่อยู่ภายในจมูก ซึ่งอาการนี้จะเกิดเนื่องจากแผลมีการดูแลรักษาที่ไม่ดี มีสิ่งสกปรกเข้าไปในแผลจนเป็นเหตุให้แผลเกิดการติดเชื้อและอักเสบได้ ซึ่งสามารถทำการรักษาได้ด้วยการทำความสะอาดแผลและให้ยาปฏิชีวนะ
การติดเชื้อในระยะกลาง คือ การติดเชื้อที่เกิดขึ้นหลังจากการผ่าตัดตั้งแต่ 1 เดือนจนถึงหลายปี ผู้ป่วยที่มีการติดเชื้อในระยะกลางจะมีอาการบวมแบบเป็น ๆ หาย ๆ บางครั้งมีอาการแสบร้อนและบวมแดงร่วมด้วย หรือมีน้ำไหลออกมาจากจมูกเป็นครั้งคราว ซึ่งสาเหตุของการอักเสบมักไม่เกี่ยวข้องกับเชื้อโรคที่มาการผ่าตัด แต่เกิดจากการอักเสบของผิวหนัง เนื้อเยื่อหรือกระดูกที่อยู่ใกล้กับแผลที่ทำการผ่าตัด เช่น การเกิดสิวอักเสบ ไซนัสอักเสบ ผิวหนังติดเชื้อ เป็นต้น เชื้อโรคที่มาจากการอักเสบดังกล่าวจะเข้ามาที่บริเวณจมูกและส่งผลให้เกิดการติดเชื้อได้ ถึงแม้ว่าการติดเชื้อแบบนี้จะไม่รุนแรงแต่ก็ต้องไปพบแพทย์เพื่อทำการรักษาให้หาย
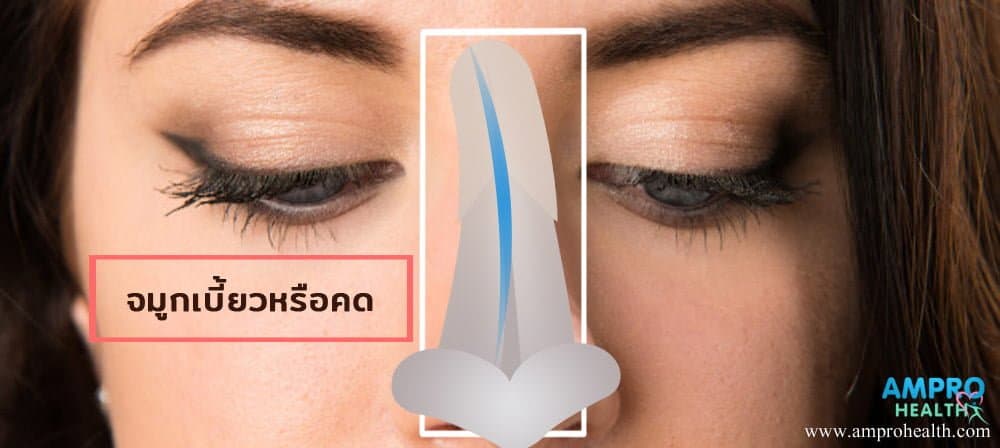
2.จมูกเบี้ยวหรือคด
การที่จมูกเบี้ยวหรือคดเป็นอาการแทรกซ้อนที่ไม่ต้องการให้เกิดขึ้นก็ตาม แต่เป็นอาการที่เกิดขึ้นได้ง่ายและพบได้บ่อยที่สุดในการ เสริมจมูก ซึ่งอาการที่เกิดขึ้นในระยะแรกไม่เกิน 2 สัปดาห์หลังจากที่ทำการเสริมจมูก อาจจะเกิดขึ้นจากการที่เนื้อเยื่อมีอาการบวม ดังนั้นเมื่ออาการบวมของกล้ามเนื้อลดลงแล้ววัสดุที่เสริมเข้าไปยังไม่อยู่ในตำแหน่งที่ต้องการ แพทย์ยังสามารถทำการเคลื่อนย้ายวัสดุดังกล่าวให้กลับเข้าสู่ตำแหน่งที่ต้องการได้ แต่ถ้าอาการจมูกเบี้ยวเกิดขึ้นนานกว่า 2 สัปดาห์หลังจากทำการผ่าตัด แพทย์จะไม่สามารถทำการเคลื่อนย้ายตำแหน่งของวัสดุที่เสริมจมูกได้ จะต้องทำการผ่าตัดเพื่อเคลื่อนย้ายวัสดุไปยังตำแหน่งที่ต้องการเท่านั้น เนื่องจากร่างกายมีการสร้างพังผืดขึ้นมายึดเนี่ยววัสดุจึงไม่สามารถขยับวัสดุดังกล่าวได้
3.ผิวหนังมีความหนาลดลง
การ เสริมจมูก ด้วยวัสดุสังเคราะห์หรือสิ่งแปลกปลอมชนิดอื่นข้าสู่จมูก วัสดุดังกล่าวจะมีการเสียดสีกับผิวหนังอยู่ตลอดเวลาส่งผลให้ผิวหนังที่มีการสัมผัสวัสดุเสริมจมูกมีขนาดที่บางลง ซึ่งจะทำให้วัสดุเกิดการทะลุออกมาจากผิวหนัง โดยเฉพาะผิวหนังบริเวณปลายจมูกที่มีการเสริมให้โด่งขึ้นจนผิวหนังในส่วนปลายจมูกตึงแน่น การแก้ไขปัญหาสำหรับผิวหนังที่มีความหนาลดลงทำให้ด้วยการลดความสูงของบริเวณปลายจมูกให้อยู่ในระดับที่พอดีให้บริเวณปลายจมูกมีเนื้อหลงเหลือในปริมาณที่สามารถปิดวัสดุไม่ให้ทะลุออกมาได้ หรืออาจใช้วัสดุจากธรรมชาติ เช่น กระดูกอ่อน เนื้อเยื่อ ของผู้เข้ารับการผ่าตัดมาใส่ในบริเวณปลายจมูก เพื่อที่ร่างกายจะทำการสร้างเนื้อเยื่อขึ้นมาคลุมส่วนปลายจมูกเพื่อลดความเสี่ยงในการทะลุของวัสดุเสริมจมูกออกมา
4.ผิวหนังทะลุ
อาการผิวหนังทะลุสามารถเกิดขึ้นได้ในทุกส่วนของจมูกที่ทำการเสริม แต่ที่พบได้บ่อยจะเกิดที่บริเวณปลายจมูก ซึ่งเมื่อเกิดอาการผิวหนังทะลุแล้วจะทำให้ผู้ป่วยมีรอยแผลเป็นเกิดขึ้นอย่างชัดเจน อาการแทรกซ้อนที่ตามมาหลังจากผิวหนังทะลุก็คือการติดเชื้อเป็นหนอง ส่งผลให้เนื้อเยื่อตาย ดังนั้นเมื่อรู้สึกว่ามีอาการปวดแสบปวดร้อนที่บริเวณจมูกควรรีบไปพบแพทย์ในทันที่เพื่อทำการถอดวัสดุจมูกออกเพื่อป้องกันไม่ให้วัสดุทะลุเนื้อออกมาจนเกิดเป็นแผลเป็นขึ้น
การผ่าตัดเพื่อนำวัสดุหรือสิ่งแปลกปลอมจากภายนอกเข้าสู่ร่างกาย มีความเสี่ยงที่ร่างกายจะเกิดปฏิกิริยาการต่อต้าน
5.สันจมูกมีลักษณะขรุขระไม่เรียบ
การที่ผิวหนังบริเวณจมูกมีลักษณะที่ขรุขระจะพบได้หลังจากที่ทำการ เสริมจมูก มากกว่า 1 ปี เนื่องจากร่างกายมีการสร้างพังผืดขึ้นมาคลุมวัสดุที่ใช้ในการเสริมจมูกหรือมีแคลเซียมมาเกาะกับวัสดุ ส่งผลให้ผิวหนังจมูกมีลักษณะเป็นคลื่น ซึ่งสามารถทำการแก้ไขด้วยการเปลี่ยนวัสดุที่ใช้ในการเสริมจมูกให้มีความอ่อนนุ่มมากกว่าเดิม
อาการแทรกซ้อนที่เกิดขึ้นสามารถเกิดขึ้นเพียงออย่างเดียวหรือเกิดขึ้นได้หลายอย่างในผู้ป่วยคนเดียว และอาการแทรกซ้อนที่เกิดขึ้นอาจเกิดขึ้นได้จากหลายปัจจัย แต่อาการแทรกซ้อนทุกอย่างสามารถป้องกันไม่ให้เกิดขึ้นได้ ซึ่งการป้องกันอาการแทรกซ้อนทำได้ดังนี้
- ความพร้อมของร่างกาย
ผู้ที่ต้องการเข้ารับการผ่าตัดเสริมจมูกต้องมีร่างกายที่แข็งแรงไม่เจ็บป่วย หรือมีโรคประจำตัวที่มีความเสี่ยงในการผ่าตัดเสริมจมูก เช่น ไซนัสอักเสบ ไข้หวัด เบาหวาน โรคหัวใจ เป็นต้น หรือมีการรับประทานยาที่ลดการแข็งตัวของเลือดหรือได้รับยาที่มีผลยับยั้งการหายของแผลที่เกิดขึ้นจากการผ่าตัดได้ เช่น การให้คีโม ยาฆ่าเชื้อมะเร็ง - สถานะทางการเงิน
ค่าใช้จ่ายในการผ่าตัดเสริมจมูกจะมีค่าใช้จ่ายจำนวนหนึ่ง ดังนั้นก่อนที่ผู้ป่วยจะเข้ารับการผ่าตัดควรเตรียมเงินให้พร้อมเพียงพอกับค่าใช้จ่ายในการผ่าตัด เพราะในการ เสริมจมูก ยิ่งใช้วัสดุที่มีคุณภาพสูง แพทย์ผู้เชี่ยวชาญและมีประสบการณ์การทำงานมายาวนาน ค่าใช้จ่ายในการผ่าตัดก็จะสูงตามไปด้วย ค่าใช้จ่ายที่สูงจะช่วยลดความเสี่ยงในการเกิดอาการแทรกซ้อนที่เป็นอันตรายต่อร่างกาย อย่าประหยัดเงินด้วยการเลือกใช้บริการกับสถานพยาบาลที่มีราคาถูกแต่ไม่มีมาตรฐานในการผ่าตัด - คลีนิก สถานบริการหรือโรงพยาบาล
การผ่าตัด เสริมจมูก ถึงแม้ว่าจะเป็นการผ่าตัดขนาดเล็กส่วนมาก แต่ก็ควรทำการเลือกสถานที่ให้บริการที่ได้มาตรฐาน มีความสะอาด ปลอดเชื้อและมีการแบ่งพื้นที่ใช้งานอย่างชัดเจน ว่าส่วนใดเป็นพื้นที่ทำการผ่าตัด ส่วนใดเป็นพื้นที่ต้อนรับผู้ป่วย ส่วนใดเป็นพื้นที่พักฟื้นของผู้ป่วย การกำหนดพื้นที่อย่างชัดเจนจะช่วยป้องกันการสะสมของเชื้อโรคและเพื่อความปลอดภัยของผู้เข้ารับการผ่าตัดจากการติดเชื้อได้มีการับรองจากหน่วยงานของรัฐบาลและกองการประกอบโรคศิลปะ จากกระทรวงสาธารณสุข มีการตรวจสอบอย่างต่อเนื่อง - แพทย์ผู้ทำการผ่าตัด
แพทย์ผู้ทำการผ่าตัด เสริมจมูก มีความสำคัญ เพราะแพทย์ผู้มีความชำนาญและเชี่ยวชาญจะสามารถทำการผ่าตัดเสริมจมูกให้ได้รูปทรงที่สวยงามตามที่ต้องการ ในขณะที่ทำการผ่าตัดแพทย์จะต้องสวมอุปกรณ์ป้องกันการติดเชื้อเพื่อป้องกันเชื้อโรคเข้าสู่ร่างกายของผู้เข้ารับการผ่าตัด และแพทย์ต้องผ่านการอบรมหลักสูตรเฉพาะทางเกี่ยวกับศัลยกรรมตกแต่งเกี่ยวกับการตกแต่งจมูก เพราะการอบรมเฉพาะทางจะช่วยให้แพทย์มีความรู้ความเข้าใจและสามารถแก้ไขปัญหาที่เกิดขึ้นจากการศัลยกรรม รวมถึงสามารถป้องกันอาการแทรกซ้อนที่อาจเกิดขึ้นได้เป็นอย่างดี - ศึกษาข้อมูล
ผู้ที่ต้องการเข้ารับการผ่าตัดควรทำการศึกษาข้อมูลเกี่ยวกับการศัลยกรรมเสริมจมูกก่อนที่จะตัดสินใจทำการผ่าตัดเสริมจมูก เพื่อป้องกันกลุ่มผู้ที่ไม่หวังดีเข้ามาหลอกลวงใช้วัสดุที่ไม่ได้คุณภาพในการเสริมจมูก ดังนั้นการศึกษาหาข้อมูลอาจจะทำการสอบถามจากผู้รู้หรืออ่านเอกสารต่าง ๆ ก่อน เพื่อเป็นประโยชน์ในการตัดสินใจเลือกวัสดุ ขั้นตอนในการผ่าตัดเสริมจมูกที่ได้ผลดีที่สุด
การผ่าตัดเพื่อศัลยกรรม เสริมจมูก สามารถเนรมิตจมูกที่สวยงามตามที่ต้องการ แต่ทุกสิ่งทุกอย่างบนโลกนี้ไม่มีอะไรที่ดีพร้อมไปเสียทุกอย่าง การศัลยกรรมก็เช่นกัน แม้จะสามารถช่วยให้มีจมูกที่สวยงามขึ้นแต่ถ้าใช้วัสดุที่ไม่ดี แพทย์ที่ไม่มีความชำนาญ หรือสถานที่ที่ไม่มาตรฐาน ผู้ป่วยก็อาจะมีอาการแทรกซ้อนเกิดขึ้น ซึ่งสามารป้องกันได้ด้วยตัวของผู้เข้ารับการผ่าตัดและแพทย์ผู้ให้การรักษานั้นเอง
อ่านบทความที่เกี่ยวข้องเพิ่มเติมตามลิ้งค์ด้านล่าง
เอกสารอ้างอิง
สมาคมแพทย์ตกแต่งเสริมสวยแห่งประเทศไทย. สวยให้สุด หยุดที่ศัลยแพทย์ตกแต่ง : กรุงเทพฯ: ไอดี ออล ดิจิตอล พริ้น จำกัด,2561.